
兴奋剂检测方法的研究进展
1964年,国际运动医学会的国际兴奋剂会议将兴奋剂的概念定义为:参加竞赛的运动员使用任何异体物质,或以不正常的量和不正常的进入机体的途径使用生理物质,试图人为地以不正当方式提高其竞赛成绩的行为。众所周知,使用兴奋剂对运动员的身体和心理都有严重的伤害。在体育竞技比赛中使用兴奋剂也是一种不道德行为,不仅不符合诚实和公平竞争的体育道德,也是对运动员誓言的背叛,和对奥林匹克宪章的亵渎。因此对兴奋剂的检测研究始终是反兴奋剂工作的重点之一。
检测仪器的发展,特别是色谱一质谱联用技术的长足进步,使得复杂生物基质中的微量成分可以被精确测定,并极大促进了兴奋剂检测手段的进步。目前,兴奋剂检测的主要方法有气相色谱、高效液相色谱、气相色谱一质谱联用、液相色谱一质谱联用副、免疫分析法、流动注射电化学发光、高效毛细管电泳、毛细管电泳一离子阱质谱等方法。本文对目前主流的兴奋剂检测方法进行了综述。
1 色谱一质谱法
色谱仪具有高效的分离能力,质谱仪可以通过直接测定物质的质量数与电荷的比值准确快速地对物质进行定性分析。色谱一质谱联用技术将色谱仪的高效分离作用与质谱仪对未知样品的准确鉴别能力相结合,是色谱技术、质谱技术与计算机技术三种现代化技术紧密结合的产物。色谱一质谱联用技术主要分为气相色谱一质谱法和液相色谱一质谱法,可被用于检测大部分兴奋剂,包括蛋白同化制剂、肽类激素、b22激动剂、有抗雌激素作用的制剂、利尿剂和其他掩蔽剂、刺激剂、麻醉剂、大麻(酚)类、糖皮质类固醇等。
1.1气相色谱一质谱法 GC - MS
由于从气相色谱柱分离后的样品呈气态,流动相也是气体,与质谱仪的进样要求相匹配,因此气相色谱仪和质谱仪最容易实现联用。气相色谱一质谱(gaschromatography - mass spectrometry,GC - MS)法综合了气相色谱和质谱的优点,弥补了各自的缺陷,具有灵敏度高、分析速度快和鉴别能力强的特点,可同时完成待测组分的分离和鉴定,特别适用于多组分混合物中未知组分的定性和定量分析,判断化合物的分子结构,准确测定化合物的分子量。
1972年慕尼黑奥运会兴奋剂检测实验室首次使用GC - MS联用仪对兴奋剂进行检测。之后,GC- MS联用技术有了长足进步,特别是毛细管气相色谱柱的使用,使GC - MS技术的分离效果和进样量有了极大改善。1984年洛杉矶奥运会的1 510份尿样全部使用GC - MS联用仪进行类固醇类兴奋剂的筛选和确证。
20世纪90年代,高分辨质谱( high resolution massspectrometry,HRMS)技术通过测量离子的精确质量,从而避开其它具有相同整数质量离子的干扰,显著降低了化学噪声,提高了测量的信噪比。采用HRMS技术检测残留激素类物质成为欧洲共同体认可的方法。Schanzer等通过检测6 700份运动员尿样中的蛋白同化雄性激素类固醇( anabolic androgenicsteroids.AAS)含量,对比研究了CC - HRMS法和GC- MS法的检测能力。采用GC - MS法仅检出41份阳性尿样,而cc - HRMS法检出了116份阳性尿样。这是由于其中75份阳性尿样属低浓度样品,用GC -MS法无法检出,采用CC - HRMS才可检出。因此,1993年在德国Stuttgart举行的世界田径锦标赛,首次将GC - HRMS法用于兴奋剂检测。1996年亚特兰大奥运会也首次采用GC - HRMS法对兴奋剂进行检测,并首次报告检出1种新的免疫刺激剂布罗曼坦( bromantan)o
2000年悉尼奥运会首次引进了气相色谱一燃烧一同位素比质谱( gas chromatography - combustion -i-sotope ratio mass spectrometer,GC -C - IRMS)法,主要用于检测内源性类固醇制剂。这种质谱技术广泛用于地质、石油等行业,用于测量目标化合物中C13和C12的比值,其原理见图1。
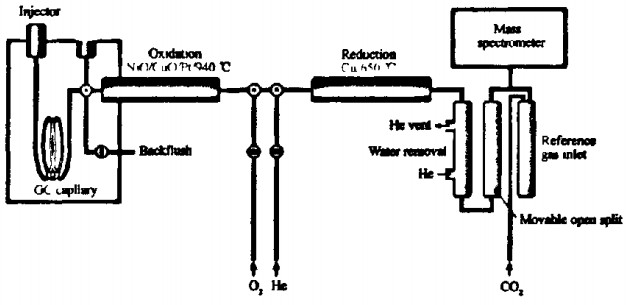
图1气相色谱一燃烧一同位素比质谱原理示意图
目标化合物经由气相色谱分离后进入氧化炉,所有碳氢化合物催化氧化成C02和H20,通过冷阱或膜除去水,C02进入质谱仪,由法拉第杯检测质量数44、45和46的信号,然后计算得出该化合物C13和C12的比值。由于人体自身合成与分泌的内源性类固醇激素C13和C12的比值与制药工业制备的类固醇制剂的同位素比不同,所以通过该法可以检测运动员是否使用了类固醇制剂。但是该方法也存在操作繁琐、费时、灵敏度低等缺点,因此,目前该方法不用于初筛,只用于可疑阳性样本的确定。
1.2液相色谱一质谱法
液相色谱—质谱(liquid chromatography - massspectrometry,LC - MS)联用技术始于20世纪70年代,1992年巴塞罗那奥运会上使用LC/MS联用仪很方便地检出刺激剂美沙卡伯( mesocarb)的代谢物,显示了LC - MS联用的优越性,但当时的接口和离子化技术限制了LC - MS联用技术在常规检测中的广泛应用。
随着20世纪80年代中后期大气压电离技术( at-mosphere pressure ionhation,API)的成熟,LC - MS联用技术得以迅速发展。LC - MS的API技术是一种软电离方式,通过调节离子源电压,可以控制离子的断裂,获取结构信息,大大拓宽了LC - MS的分析范围,可被用来分析蛋白质和脱氧核糖核酸等生物大分子。在兴奋剂检测领域,LC - MS法不仅可以检测刺激剂等小分子兴奋剂,也可以对肽类激素和蛋白质等大分子兴奋剂进行检测。
针对刺激剂利他林及其主要代谢物利他林酸,陆江海等利用固相萃取一液相色谱一串联质谱法建立了检测它们在人尿中含量的方法。他们将尿样中的药物经反相C18固相萃取柱净化、氮气吹至干,以甲睾为内标,用流动相溶解后进行液相色谱一串联质谱法测定。研究表明,该方法的最低检出限为5μgL-l,利他林和利他林酸的回收率分别为80.6%和68. 4%,批内和批间的相对标准偏差小于6.O%,满足国际反兴奋剂机构对其最低检测能力500 μg.L-l的要求。
在体内主要以代谢产物形式存在的禁用药物,如合成类固醇、刺激剂、麻醉剂和B2阻断剂等,LC - MS可以通过测定葡萄糖醛酸甙或硫酸酯结合物来确定药物的代谢情况,从而实现对这些药物的定量测定。另外,一些采用GC -MS法检测结果不理想的甾体化合物、糖皮质激素等也可采用LC - MS检测,并且检出限可以达到世界反兴奋剂委员会的最低检出限水平。2004年雅典奥运会就采用了液相色谱一离子阱质谱技术分析检测糖皮质激素。
对于肽类激素和蛋白质检测通常采用的是免疫检测方法,但随着LC - MS技术的成熟,样品前处理技术以及仪器的选择性和特异性的不断提高,不少基于LC - MS - MS的检测方法也被用于检测肽类激素和蛋白质。蛋白质通过酶解后产生多个肽段,经液相色谱分离后用串联质谱获得肽的质量谱,从而对肽段进行鉴别和测定。通过蛋白质序列数据检索,得出蛋白质序列信息,从而实现对蛋白质的快速高灵敏度的鉴别和测定。
目前,由于LC - MS技术的不同电离源对不同类型物质的电离条件各不相同,受液相色谱条件影响大,裂解信息少,往往需要测定多级裂解的谱图才能达到鉴别的目的。因此谱图解析技术的不成熟和较高的仪器成本,导致LC - MS技术的普及性还不及GC- MS技术。


文章评论